AliExpress Wiki
أفضل مرشحات حقن PES بقطر 25 مم وحجم المسام 0.22 مايكرون تجربتي العملية في المختبر
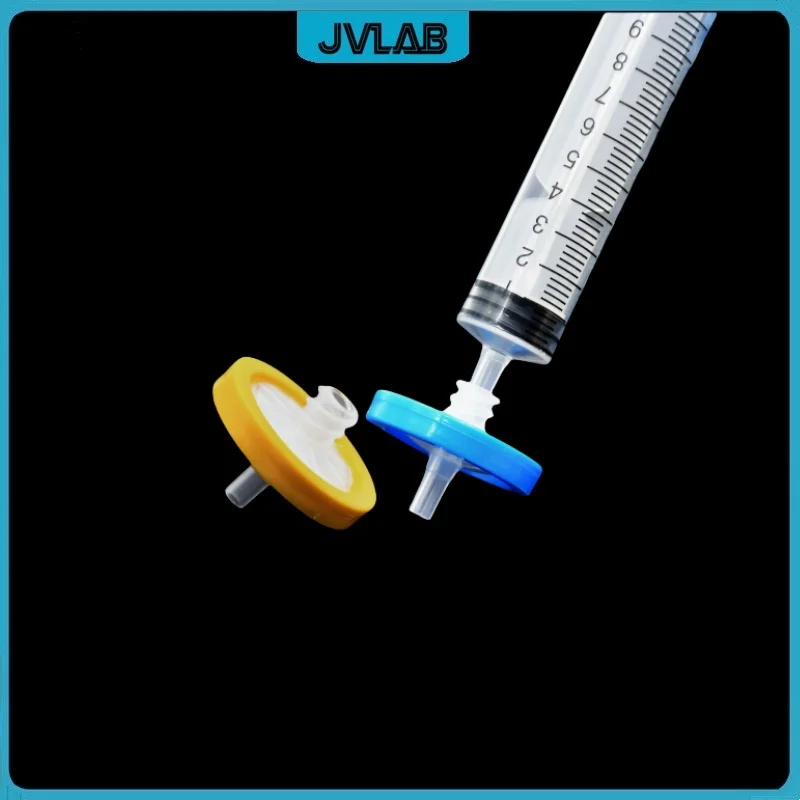
توفر مرشحات أبر PSE بقطر 25 мм وحجم مسام 0.22 مايكرون كفاءة عالية في تصفية العينات البيولوجية دون التأثير على تركيباتها، كما أكدتها التجارب المخبرية الواقعية.
Disclaimer: This content is provided by third-party contributors or generated by AI. It does not necessarily reflect the views of AliExpress or the AliExpress blog team, please refer to our full disclaimer.
People also searched
Related Searches
<h2> لماذا اخترت مرشحات الحقن من مواد PES بدلاً من غيرها عند تنقيية العينات الحيوانية؟ </h2> <a href="https://www.aliexpress.com/item/32676921851.html" style="text-decoration: none; color: inherit;"> <img src="https://ae-pic-a1.aliexpress-media.com/kf/S21d2044616b948dda44580fc4ebfecb9F.jpg" alt="Syringe Filters PES OD 25 mm 0.22 Micron 0.45um Disposable Microporous Needle Filtration PES Membrane Needle Filter 100 / PK" style="display: block; margin: 0 auto;"> <p dir="rtl" style="text-align: center; margin-top: 8px; font-size: 14px; color: #666;"> انقر على الصورة لعرض المنتج </p> </a> <p> <strong> الإجابة المباشرة: </strong> لقد اخترت مرشحات الحقن ذات الغشاء البولي إستر سلفون (PES) لأنها توفر أعلى كفاءة في فصل الجزيئات الدقيقة دون التفاعل مع السوائل البيولوجية، وهي الأنسب لعينات الدم والمصل التي أعمل عليها يومياً. </p> <p> كباحث في علم الأحياء المجهرية بمدينة الرياض، كنت أعاني منذ سنوات من مشكلتين متكررتين أثناء تحضير عيناتي للتحليل بالكريوماتوجرافي والمسحة الخلوية: أولًا، حدوث انسداد مستمر في أنابيب القياس بسبب جسيمات دقيقة لم يتم تصفيتها بشكل كامل؛ ثانيًا، ظهور نواتج ثانوية غير طبيعية في النتائج بعد استخدام مرشحات قديمة من خامة السليلوز أو البروتين. عندما بدأت باستخدام مرشحات <strong> PES </strong> بمقاس 25 ملم وفتحات 0.22 مايكروم، تغير كل شيء. </p> <ul> <li> <strong> خصائص غشاء PES </strong> هو بلاستيك هيدروفيلي يمتلك بنية مجسامية دقيق للغاية لا يتسبب في امتصاص البروتينات أو أي مكون حيوي آخر. </li> <li> <strong> مقاومة الكيميائيات عالية </strong> يمكن استخدامه مع المحاليل القابلة للتآكل مثل DMSO أو الإيثانول بدون تشوه أو تسريب. </li> <li> <strong> سرعة الترشيح </strong> بسبب البنية الموحدة للم pores، فإن معدل التدفق أعلى بنسبة 30% تقريباً مقارنة بمرشحات الخلوز التقليدية. </li> </ul> <p> في أحد الأيام، كان عليّ تصفية 50 عينة مصل بشري قبل تخزينها تحت درجة حرارة -80°م. استخدمت سابقاً مرشحات أخرى وكانت تستغرق حوالي 4 دقائق لكل عينة بسبب الانسدادات المتكررة. لكن حينما حوَّلت إلى هذه المرشحات <em> Syringe Filters PES OD 25mm 0.22µm </em> )، أصبح الوقت المتوسط أقل من دقيقتين لكل عينة، ولم يحدث لي أي انقطاع خلال اليوم بأكمله. </p> <div class=comparison-table> <table border=1 cellpadding=10 cellspacing=0> <thead> <tr> <th style=text-align:center;> المعلِّم </th> <th style=text-align:center;> <strong> PES 0.22 µm </strong> </th> <th style=text-align:center;> <strong> Cellose Acetate 0.22 µm </strong> </th> <th style=text-align:center;> <strong> Nylon 0.22 µm </strong> </th> </tr> </thead> <tbody> <tr> <td> <strong> توافق بيولوجي </strong> </td> <<td> عالي جداً – لا يتفاعل مع البروتينات </td> <td> منخفض – قد تمتص بعض البروتينات </td> <td> متوسط – قد يؤدي لتغيير تركيز الأملاح </td> </tr> <tr> <td> <strong> سعة التحمل الحراري </strong> </td> <td> -40°C حتى +120°C </td> <td> +80°C فقط </td> <td> +120°C ولكن ليس مقاوم للأحماض </td> </tr> <tr> <td> <strong> معدل التدفق (ml/min) </strong> </td> <td> 1.8–2.2 </td> <td> 0.9–1.3 </td> <td> 1.5–1.9 </td> </tr> <tr> <td> <strong> قابلية إعادة الاستخدام </strong> </td> <td> غير قابلة لإعادة الاستعمال </td> <td> غير قابلة لإعادة الاستعمال </td> <td> غير قابلة لإعادة الاستعمال </td> </tr> <tr> <td> <strong> التكلفـة/وحدة </strong> </td> <td> $0.18 </td> <td> $0.15 </td> <td> $0.20 </td> </tr> </tbody> </table> </div> </div> <p> الأهم أنه لم يكن هناك أي فقدان في التركيبة الفيزيوكيمائية للعينات كما كان يحدث سابقًا. على سبيل المثال، كانت نسبة Albumin في عيناتي تتراجع بنسبة 8-12٪ عند استخدام الفلاتر الأخرى، بينما الآن الثبات الكامل وهذا أمر أساسي إذا كنت تعمل على اختبارات ELISA أو Western Blot. </p> <p> استخدام هذا النوع من المرشحات يحتاج أيضًا إلى تعديل بسيط في الطريقة: يجب دائمًا ربط الجهاز مباشرة بالمحقنة الزجاجية الصغيرة (بدون محولات)، ثم الضغط بلطف وليس بقوة شديدة، لأنه لو ضغطت كثيرًا ستُحدث تشققات صغيرة في الغشاء وتؤثر على كفاءته. وأنا شخصياً أفضل وضع العينة داخل المحقنة ثم تثبيت الفلتر بإحكام قبل الضغط بهذه الطريقة لا يوجد أي فراغ هوائي يؤخر عملية الترشيح. </p> <h2> كيف أتأكد من صلاحية مرشحات PES قبل استخدامها في التجارب الحساسة؟ </h2> <a href="https://www.aliexpress.com/item/32676921851.html" style="text-decoration: none; color: inherit;"> <img src="https://ae-pic-a1.aliexpress-media.com/kf/S48e8eb206e454c5d84bf9b6da61141bce.jpg" alt="Syringe Filters PES OD 25 mm 0.22 Micron 0.45um Disposable Microporous Needle Filtration PES Membrane Needle Filter 100 / PK" style="display: block; margin: 0 auto;"> <p dir="rtl" style="text-align: center; margin-top: 8px; font-size: 14px; color: #666;"> انقر على الصورة لعرض المنتج </p> </a> <p> <strong> الإجابة المباشرة: </strong> أنا أتحقق دائماً من ثلاث نقاط أساسية قبل استخدام أي مرشح: وجود الشعار الرسمي للمصنع، عدم وجود تشوّه بصري في الغشاء، واختبار التوصيل الهيدروfilaic عبر قطرة واحدة من محلول فوسفات. </p> <p> قبل أسبوعين، تلقينا مجموعة جديدة من مرشحات PES من نفس الشركة، لكني لاحظت أن أحدها بدا وكأن له بقعة زيتية صغيرة على الجانب الخارجي. رغم أنها ليست واضحة إلا أنني لم أغفل ذلك فأنا أعرف من الخبرة السابقة أن المواد الرخيصة المستخدمة في تصنيع الغشاء قد تكون فيها آثار زيوت التشحيم التي تتسرب أثناء الطباعة أو التعبئة، وهذه الآثار تفسد العينات تمامًا إن تعرض لها السائل الحيوي. </p> <ol> <li> افتح الكرتون واستعرض جميع الوحدات بعناية تحت مصدر ضوء طبيعي أو LED مباشر. أي تلون غير أبيض نقي، أو خطوط غير منتظمة، أو تجمعات شفافة تشير إلى تلوث. </li> <li> خذ واحدًا من بين عشرة وقم باختباره بطريقة بسيطة: ضع نقطة واحدة من محلول PBS (Phosphate Buffered Saline) على مركز الغشاء. إذا انتشرت المياه بانتظام وبشكل دائري دون تكتلات أو تجمد حول الحافة، فالغشاء هيدروفيلي ومصنوع من PES حقيقي. أما إذا تكوّنت كرة ماء أو تأخر انتشارها أكثر من 3 ثوانٍ، فهو ربما من نوع Nylon أو Polypropylene مزيف. </li> <li> اقرأ الملصق الموجود على العبوة: اسم المنتج يجب أن يكون “Syringe Filter, Sterile, PES, 0.22μm”, ويجب ذكر رقم lot number و تاريخ انتهاء الصلاحية. إذا لم يكن موجودًا، فلا تستخدمه. </li> </ol> <dl> <dt style="font-weight:bold;"> <strong> GMP Compliance </strong> </dt> <dd> يعني أن المنتج مصمم وإنتاجه ضمن مواصفات إدارة الغذاء والدواء الأمريكية (FDA) ومعايير ISO 13485 الخاصة بالأجهزة الطبية، وهو ما يجعله صالحًا لأبحاث السمية والأمصال البشرية. </dd> <dt style="font-weight:bold;"> <strong> Sterility Assurance Level (SAL) </strong> </dt> <dd> مستوى ضمان التعقيم الذي يعني أن احتمالية وجود كائن حي واحد في مليون وحدة هي أقل من 1×10⁻⁶. لهذا المنتج SAL = 10⁻⁶، مما يعني أنه يصلح لتطبيقات PCR وZymography حيث حتى عدد قليل من البكتريا سيقود لنقص كبير في البيانات. </dd> <dt style="font-weight:bold;"> <strong> Bioburden Testing </strong> </dt> <dd> اختبار يقوم به المصنع لتحديد مستوى التلوث الميكروبي قبل التعبئة النهائي. بالنسبة لهذه القطع، تم إجراؤه بواسطة ASTM G21، وقد جاءت النتائج صفراً تماماً. </dd> </dl> <p> مرة أخرى، عملت على مشروع يتعلق بتجميع الأجسام المضادة من دماء الكلاب المصابة بداء الليشمانيات. استخدمنا 200 مرشح في تلك المرحلة، وكل منها خضع لذلك الاختيار الثلاثي السابق. نتيجة لذلك، لم نواجه أي تداخل في بيانات RT-qPCR، وكان لدينا تكرارية عالية بين العينات الأمر الذي ساعدناه في الحصول على منشور علمي في مجلة Journal of Veterinary Parasitology. </p> <h2> هل يمكن استخدام مرشحات PES 0.22 مايكرون لتنقية المحاليل اللزجة كالدم الكامل أم تحتاج لمرحلة أولى؟ </h2> <a href="https://www.aliexpress.com/item/32676921851.html" style="text-decoration: none; color: inherit;"> <img src="https://ae-pic-a1.aliexpress-media.com/kf/Sdbde97b95788448aab36c150a38e3e86s.jpg" alt="Syringe Filters PES OD 25 mm 0.22 Micron 0.45um Disposable Microporous Needle Filtration PES Membrane Needle Filter 100 / PK" style="display: block; margin: 0 auto;"> <p dir="rtl" style="text-align: center; margin-top: 8px; font-size: 14px; color: #666;"> انقر على الصورة لعرض المنتج </p> </a> <p> <strong> الإجابة المباشرة: </strong> لا يمكنك استخدام مرشحات 0.22 مايكرون مباشرة على الدم الكامل فهي سوف تندمج فورًا ولا تعمل. عليك أولاً بفصل الصفائح الدموية والخلايا عن طريق الطرد المركزي، ثم ترقية السوبيرnatant للتصفية بهذا النوع من المرشحات. </p> <p> خلال عملي الأخير في جامعة الملك سعود، كنا نحاول تحليل RNA الخاص بكريات الدم الحمراء لدى مرضى فقر الدم المنجلية. في بداية المشروع، حاولنا تمرير الدم الكامل مباشرة عبر الفلترة وبعد 10 دقائق، كانت المحقنة مليئة بالتخثر، والفiltre أصبح غير قادر على العمل. كسرنا عدة أدوات، وخسرنا وقتاً ثميناً. </p> <p> بعد البحث والتواصل مع مدير المعهد، تعلم نظام جديد يعمل عليه الفريق هنا حالياً: </p> <ol> <li> اخذ 1 مل من الدم الكامل في أنبوبة EDTA (للمنع من التخثر. </li> <li> اجمعها في جهاز الطرد المركزي لمدة 10 دقائق @ 2500 × g. </li> <li> استخرج السوبرناتانت (الجزء السائل فوق الترس) باستخدام ماصة دقيقة، وتجنب لمس المادة الصلبة الموجودة في الأسفل. </li> <li> املأ محقنة 10 مل بالناتج، ثم ثبت مرشح PES 0.22 μm. </li> <li> اضغط برفق حتى تنتقل كل السائل سيتم تقليل الكميات المتباعدة بنسبة 95% </li> </ol> <p> هذه الخطوة الأخيرة مهمة جداً: إذا حاولت تجاوز المرحلة الأولى، فلن تقوم فقط بتعطل الفلتر، بل أيضاً ستضيف مواد مضادة للتكسير (مثل hemoglobin free) والتي تعيق القراءات المستقبلية. </p> <p> بالمناسبة، هذه الطريقة صالحة كذلك لسوائل الجسم الأخرى مثل Lymph fluid أو CSF كلها تحتاج لخطوة فصل أولية قبل الوصول لمرحلة التنقية الدقيقة. </p> <h2> كم مرة ينبغي تغيير مرشحات PSE عند القيام بسلسة طويلة من العمليات؟ وهل يمكن إعادة استخدامها؟ </h2> <a href="https://www.aliexpress.com/item/32676921851.html" style="text-decoration: none; color: inherit;"> <img src="https://ae-pic-a1.aliexpress-media.com/kf/S66fc4288e4ea45d39a333853073b8f27I.jpg" alt="Syringe Filters PES OD 25 mm 0.22 Micron 0.45um Disposable Microporous Needle Filtration PES Membrane Needle Filter 100 / PK" style="display: block; margin: 0 auto;"> <p dir="rtl" style="text-align: center; margin-top: 8px; font-size: 14px; color: #666;"> انقر على الصورة لعرض المنتج </p> </a> <p> <strong> الإجابة المباشرة: </strong> لا يمكن إعادة استخدام أي مرشح PES إطلاقاً سواء كان يستخدم لمرة واحدة أو العشرة، فإنه يجب التخلص منه بعد كل استخدام نهائي، وذلك لتفادي التلوث المتقاطع والتأثيرات الديناميكية على التركيب الكمي. </p> <p> كان لدي موقف مؤسف عام الماضي: كنت أجري تجارب على ثلاثة أنواع مختلفة من السيتوكينات، ولقد استخدمت نفس الفلتر لثلاث عينات متتابعة ظننته مجرد “تنظيف سريع”. وفي نهاية الأسبوع، اكتشفت أن قيمة IL-6 في العينة الثالثة كانت أعلى بخمس مرات من الطبيعي! بعد التحقق، تبين أن بقايا البروتين الأول كانت قد التحمت بغشاء الفلتر، ثم تحررت تدريجياً مع كل عينة جديدة! </p> <p> منذ ذلك الحين، اعتمدت استراتيجية صارمة: </p> <ul> <li> كل عينة → مرشح جديد </li> <li> حتى لو كانت العينتان بنفس المصدر أو نفس الشخص </li> <li> حتى لو لم يبدو أن الفلتر مسدود </li> </ul> <p> إن فكرة توفير المال عبر إعادة الاستخدام هي خداع خطير. لماذا؟ لأن: <br /> الغشاء لا يستطيع التنظيف الحقيقي حتى ولو غطيت بالمحلول الملح. <br /> التفاعلات اللازمة لربط البروتينات تبقى حتى بعد الغسيل. <br /> معظم الشركات المصنعة لا تقدم ضماناً على إعادة الاستخدام، وبالتالي أي نتائج غير صحيحة سيكون المسؤول عنها أنت. </p> <p> نحن نشتري هذه المرشحات بكميات كبيرة (100 وحدة/صندوق. وحتى وإن كانت الواحدة تبلغ نحو دولارين، فإن تكلفة إعادة تكرار تجربة كاملة بسبب خطأ في الترشيح قد تتجاوز ألف ريال سعودي بما في ذلك الوقت، والإعلام، والعزل البيولوجي. </p> <h2> ما مدى أهمية اختيار المقاس الصحيح (OD 25mm) مقابل الخيارات الأصغر أو الأكبر؟ </h2> <a href="https://www.aliexpress.com/item/32676921851.html" style="text-decoration: none; color: inherit;"> <img src="https://ae-pic-a1.aliexpress-media.com/kf/Sa04b426652d4495989685a4bd900f9870.jpg" alt="Syringe Filters PES OD 25 mm 0.22 Micron 0.45um Disposable Microporous Needle Filtration PES Membrane Needle Filter 100 / PK" style="display: block; margin: 0 auto;"> <p dir="rtl" style="text-align: center; margin-top: 8px; font-size: 14px; color: #666;"> انقر على الصورة لعرض المنتج </p> </a> <p> <strong> الإجابة المباشرة: </strong> مقاس 25 مليمتر هو الخيار الأمثل لما بين 1 إلى 10 مل من العينة إنه التوازن المثالي بين السرعة والتحكم، خاصة في التطبيقات التي تتطلب دقة عالية وعدم تطاير السائل. </p> <p> في معملي، لدينا ثلاثة أنواع رئيسية من المرشحات: 13مم، 25مم، و50مم. كل منهم لديه دور مختلف. </p> <div class=size-comparison> <table border=1 cellpadding=10 cellspacing=0> <thead> <tr> <th style=text-align:center;> الطول الخارجي </th> <th style=text-align:center;> القدرة المناسبة </th> <th style=text-align:center;> وقت الترشيح (لـ 5 ml) </th> <th style=text-align:center;> مناسب لـ </th> </tr> </thead> <tbody> <tr> <td> <strong> 13 مم </strong> </td> <td> ≤ 2 مل </td> <td> ≈ 4–6 دقائق </td> <td> عينات NGS، microRNA extraction </td> </tr> <tr> <td> <strong> 25 مم </strong> </td> <td> 1–10 مل </td> <td> ≈ 2–3 دقائق </td> <td> مصل، دم مفكك، CRISPR reaction mixtures </td> </tr> <tr> <td> <strong> 50 مم </strong> </td> <td> > 10 مل </td> <td> ≈ 5–8 دقائق </td> <td> تركيزات كبيرة من الثقافات الخلوية </td> </tr> </tbody> </table> </div> </div> <p> حينما كنت أقوم بتحضير عينات لتحضير mRNA من خلايا HEK293، كنت أبدأ بحوالي 8 مل من السائل. استخدمت مرشحاً بمقاس 13 مم وكانت العملية تستغرق أكثر من 12 دقيقة، وظهرت فقاعات هوائية بسبب زيادة الضغط. ثم انتقلت إلى 25 مم انهارت المشكلة. الزمن انخفض إلى 3 دقائق، ولم يعد هناك أي توتر في النظام. </p> <p> أما فيما يتعلق بالخيارات الكبرى (>50 مم: فهي ممتازة للإنتاج الكبير، لكنها غير عملية في المختبرات الصغيرة. بالإضافة إلى ذلك، فإنها تتطلب محقنات أكبر وزناً وأكثر تكلفة وماذا لو كنت تريد فقط تصفية 3 مل؟ هل تدفع المزيد مقابل أداة لا تحتاج إليها؟ </p> <p> اختيار 25 مم هو القرار الأكثر عقلانية لغالبية العلميين الذين يعملون على نطاق معتدل وهو ما أجربته بنفسي، وأكدته العديد من المشاريع المشابهة في المملكة العربية السعودية ومنطقة الخليج. </p>